藍軟坊銷售管理軟件 直觀高效,助力企業(yè)銷售全流程管理
在當今競爭激烈的市場環(huán)境中,一套功能強大且界面直觀的銷售管理軟件已成為企業(yè)提升效率、驅(qū)動業(yè)績增長的核心工具。藍軟坊銷售管理軟件正是為此而生,它不僅集成了客戶管理、銷售跟蹤、數(shù)據(jù)分析等核心功能,更以其清晰、高效、人性化的操作界面,為企業(yè)銷售團隊帶來卓越的使用體驗。以下,我們將通過其界面預覽,深入解讀其如何賦能軟件銷售與企業(yè)管理。
一、整體布局:簡潔清晰,一目了然
藍軟坊銷售管理軟件的主界面采用了現(xiàn)代化、模塊化的設計風格。色彩搭配以商務藍、科技灰為主,沉穩(wěn)而專業(yè),視覺焦點突出。界面頂部為全局導航欄,集成了【儀表盤】、【客戶】、【商機】、【訂單】、【報表】、【設置】等核心模塊,用戶可以輕松一鍵切換,無需深入多層菜單。中央?yún)^(qū)域是動態(tài)信息展示區(qū),默認顯示“銷售儀表盤”,關鍵數(shù)據(jù)如銷售漏斗、業(yè)績趨勢、待辦任務等以圖表和卡片形式直觀呈現(xiàn),讓管理者對銷售全局瞬間掌握。
二、核心模塊界面深度解析
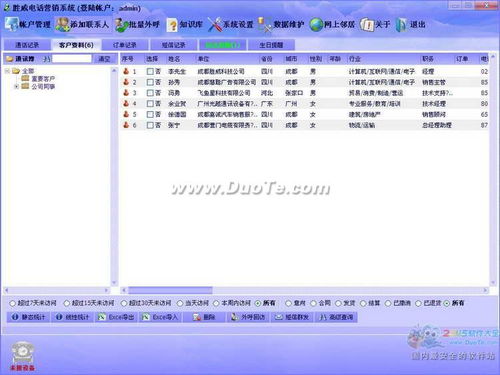
1. 客戶管理界面:
進入【客戶】模塊,界面左側(cè)為篩選與分組欄,支持按行業(yè)、規(guī)模、來源、跟進狀態(tài)等多維度快速篩選客戶。右側(cè)主區(qū)域以列表或卡片視圖展示客戶信息,關鍵字段如公司名稱、聯(lián)系人、最近聯(lián)系時間、商機階段等排列有序。點擊任一客戶,可彈出或跳轉(zhuǎn)至詳情頁,完整記錄客戶溝通歷史、購買記錄、相關文檔,實現(xiàn)了客戶信息的集中化、可視化管理,為銷售人員的精準跟進提供了堅實基礎。
2. 銷售漏斗(商機管理)界面:
【商機】模塊是軟件的核心亮點之一。界面通常以直觀的“管道圖”或“看板”形式展示銷售漏斗全貌。每個商機階段(如初步接觸、需求分析、方案報價、談判、成交)作為一個獨立列,商機卡片可在不同階段間拖拽,實時更新進展。每張卡片清晰顯示商機金額、預計成交時間、負責人及當前狀態(tài)。這種可視化設計讓團隊對每筆生意的進程了如指掌,便于管理者進行預測和資源調(diào)配。
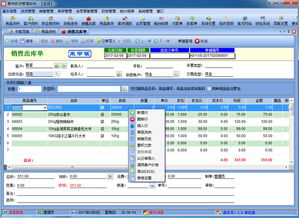
3. 訂單與合同管理界面:
在【訂單】模塊,界面設計注重流程的順暢性。從報價單生成、合同審批到訂單創(chuàng)建、發(fā)貨跟蹤、回款記錄,形成完整的閉環(huán)。列表視圖清晰列明訂單編號、客戶、金額、狀態(tài)、開票情況等。關聯(lián)性設計出色,從任一訂單可快速追溯到對應的客戶、商機及所有往來溝通,極大提升了內(nèi)部協(xié)作與對賬效率。
4. 數(shù)據(jù)分析與報表界面:
【報表】模塊提供了豐富的預置報表和強大的自定義功能。界面以圖表(柱狀圖、折線圖、餅圖)和數(shù)據(jù)表格為主,可直觀展示個人/團隊業(yè)績排行、產(chǎn)品銷量分析、回款周期、客戶來源分析等關鍵指標。用戶可通過拖拽字段輕松生成個性化看板,所有數(shù)據(jù)均實時更新,為銷售決策提供即時、可靠的數(shù)據(jù)支持。
三、針對“軟件銷售”場景的專項優(yōu)化
藍軟坊銷售管理軟件充分考慮了軟件行業(yè)銷售周期長、決策鏈復雜、版本迭代快等特點,在界面中進行了針對性優(yōu)化:
- 版本與許可管理集成: 在客戶與訂單詳情中,可清晰關聯(lián)軟件的具體版本、授權數(shù)量、許可密鑰及到期日期,并設有自動續(xù)費提醒功能。
- 演示與試用跟蹤: 商機卡片中可便捷記錄演示安排、試用賬號開通狀態(tài)及客戶反饋,幫助銷售系統(tǒng)化推進POC(概念驗證)流程。
- 知識庫快速調(diào)用: 在跟進客戶時,側(cè)邊欄或浮動窗口可直接調(diào)用產(chǎn)品白皮書、技術文檔、常見問題等知識庫內(nèi)容,方便銷售隨時解答專業(yè)問題。
四、用戶體驗與交互設計
軟件界面交互流暢,響應迅速。支持鍵盤快捷鍵、批量操作、數(shù)據(jù)導入導出。搜索功能強大,支持全局模糊搜索,快速定位任意客戶、商機或訂單。通知中心集中顯示任務提醒、審批請求、客戶動態(tài),確保重要信息無一遺漏。界面布局支持一定程度的自定義,用戶可根據(jù)角色和習慣調(diào)整常用模塊的顯示順序。
###
總而言之,藍軟坊銷售管理軟件通過其科學規(guī)劃的界面布局、直觀可視化的數(shù)據(jù)呈現(xiàn)、以及深度契合軟件銷售業(yè)務流程的細節(jié)設計,成功地將復雜的管理流程轉(zhuǎn)化為簡潔高效的操作體驗。它不僅是一套管理工具,更是提升銷售團隊戰(zhàn)斗力、驅(qū)動企業(yè)數(shù)字化增長的視覺化指揮中心。對于尋求規(guī)范化、精細化銷售管理的軟件企業(yè)而言,其界面預覽所展現(xiàn)的專業(yè)性與易用性,無疑是一個強有力的價值承諾。
如若轉(zhuǎn)載,請注明出處:http://www.golana.cn/product/42.html
更新時間:2026-03-28 00:41:20